для врачей при поддержке ведущих
медицинских вузов Санкт-Петербурга
образовательнный
портал для врачей
Мазуров В.И., Трофимов Е.А., Гайдукова И.З.
ФГБОУ ВО «Северо-Западный государственный медицинский университет имени И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия
191015, Санкт-Петербург, ул. Кирочная, 41
Псориатический артрит (ПсА) – хроническое воспалительное заболевание суставов, позвоночника и энтезисов, ассоциированное с псориазом. Патологический процесс локализуется преимущественно в тканях опорно-двигательного аппарата и приводит к развитию эрозивного артрита, внутрисуставного остеолиза. ПсА возникает у 5–7% больных среднетяжелым псориазом. Несмотря на успехи в лечении псориаза и ПсА базисными противовоспалительными препаратами (БПВП) и генно-инженерными биологическими препаратами (ГИБП), до конца не решены проблемы, связанные с иммуногенностью, наличием инфекционных осложнений, вторичной неэффективностью.
Эти факторы послужили причиной поиска новых таргетных синтетических препаратов (блокаторы сигнальных путей). К данной группе препаратов относится апремиласт, ингибитор фосфодиэстеразы 4. Полученные к настоящему времени данные
контролируемых исследований свидетельствуют о том, что препарат эффективен и безопасен при лечении псориаза и ПсА. Перспективы применения апремиласта при ПсА связаны с возможностью использования его у пациентов с неэффективностью БПВП или ГИБП, способностью поддержания длительной (более 3 лет) ремиссии, уменьшения проявлений энтезита и дактилита.
Ключевые слова: псориаз; псориатический артрит; апремиласт; фосфодиэстераза; таргетная терапия.
Контакты: Вадим Иванович Мазуров; maz.nwgmu@yandex.ru
Для ссылки: Мазуров ВИ, Трофимов ЕА, Гайдукова ИЗ. Место ингибитора фосфодиэстеразы 4-го типа в стратегии лечения псориатического артрита. Современная ревматология. 2018;12(1):41–46.
The place of a phosphodiesterase 4 inhibitor in the treatment strategy for psoriatic arthritis
Mazurov V.I., Trofimov E.A., Gaydukova I.Z.
I.I. Mechnikov North-Western State Medical University, Ministry of Health of Russia, Saint Petersburg, Russia
41, Kirochnaya St., Saint Petersburg 191015
Psoriatic arthritis (PsA) is a chronic inflammatory disease of the joints, spine, and entheses, which is associated with psoriasis. The pathological process is localized mainly in the tissues of the locomotor system and leads to the development of erosive arthritis and intra-articular osteolysis. PsA occurs in 5–7% of patients with moderate psoriasis. Despite advances in the treatment of psoriasis and PsA with diseasemodifying
antirheumatic drugs (DMARDs) and biological agents (BAs), the problems associated with immunogenicity, infectious complications, and secondary inefficiency have not been fully solved. These factors have motivated the search for novel targeted synthetic drugs (signaling pathway inhibitors). This group of drugs includes apremilast, a phosphodiesterase 4 inhibitor. Recent data of controlled studies suggest that the
drug is effective and safe in treating psoriasis and PsA. Prospects for the use of apremilast in PsA are associated with the possibility to use the drug in patients because of the inefficacy of DMARDs or BAs and with the ability to maintain long-term (more than 3-year) remission and to reduce the manifestations of enthesitis and dactylitis.
Keywords: psoriasis; psoriatic arthritis; apremilast; phosphodiesterase; targeted therapy.
Contact: Vadim Ivanovich Mazurov; maz.nwgmu@yandex.ru
For reference: Mazurov VI, Trofimov EA, Gaydukova IZ. The place of a phosphodiesterase 4 inhibitor in the treatment strategy for psoriatic arthritis. Sovremennaya Revmatologiya=Modern Rheumatology Journal. 2018;12(1):41–46.
DOI: http://dx.doi.org/10/14412/1996-7012-2018-1-41-46
Псориатический артрит (ПсА) – хроническое воспалительное заболевание суставов, позвоночника и энтезисов, ассоциированное с псориазом. Патологический процесс локализуется преимущественно в тканях опорно-двигательного аппарата и приводит к развитию эрозивного артрита, внутрисуставного остеолиза и спондилоартрита. Псориаз выявляется у 1–3% населения. Мужчины и женщины страдают псориазом одинаково часто. ПсА развивается у 5–7% больных псориазом [1, 2]. Дебют заболевания может наблюдаться в любом возрасте, но чаще приходится на 20–50 лет [1–4].
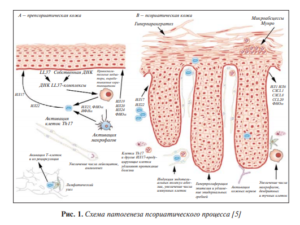
Этиология и патогенез ПсА до конца не изучены
(рис. 1) [5]. Обнаружена связь псориаза с HLA-антигенами
В13, В16, В17, В27, В38, В39, DR4, DR7. Установлено, что
HLA-B27 ассоциируется с поражением осевого скелета
(позвоночника и крестцово-подвздошных сочленений),
DR4 – с эрозивным артритом периферических суставов,
HLA-Cw6 – с ранним началом заболевания, HLA-B27, B39
и ФНОα1 -308-аллели – с прогрессированием заболевания, полиморфизм гена рецептора к интерлейкину (ИЛ) 23 (ИЛ23R) – с ПсА [6–12].
1
ФНОα – фактор некроза опухоли α.
Провоцировать появление первых признаков болезни
могут инфекционные агенты (стрептококк, стафилококк,
грибковая инфекция, ВИЧ и другие ретровирусы), эндокринные факторы (пубертатный период и период менопаузы,беременность), заболевания желудочно-кишечного тракта –ЖКТ (гастрит, холецистит, дисбактериоз кишечника), психоэмоциональный
стресс, прием лекарственных средств (препараты лития, бета-адреноблокаторы, аминохинолиновыесредства, иногда нестероидные противовоспалительные
препараты – НПВП) [1, 10].
Ведущая роль в развитии заболевания отводится иммунным механизмам [6, 11]. При псориазе наблюдается нарушение развития и функционирования определенной популяции Т-лимфоцитов с последующим высвобождением провоспалительных цитокинов и хемокинов, этот постоянный процесс формирует «порочный круг» в развитии псориаза [6–12].
Результаты иммуногистохимических исследований кожи
больных псориазом показали, что инфильтрация
Т-клетками предшествует клиническим проявлениям на
коже. В клеточных инфильтратах кожи при этом выявляется повышенное содержание CD4+ и CD8+ лимфоцитов с преобладанием последних [6].
ИЛ12 вырабатывается макрофагами и дендритными
клетками и играет важную роль в функционировании врожденнойиммунной системы, контролируя дифференцировку CD4+ лимфоцитов в подкласс Т-хелперов 1-го типа (Th1).
Th1-клетки продуцируют провоспалительные цитокины:
ФНОα и интерферон γ (ИФНγ). ИЛ12 также индуцирует
кожные лимфоцитарные антигены, вызывая миграцию
Т-клеток в кожу и активирует CD8+ (цитотоксические)
Т-клетки и естественные киллеры [1, 6, 9–11].
ФНОα играет одну из ключевых ролей в патогенезе псориаза, стимулируя синтез других провоспалительных цитокинов, значение которых в развитии болезни установлено. Кроме того, он способствует накоплению воспалительных клеток в тканях путем индукции экспрессии молекул внутриклеточной адгезии
1 (ICAM1) и повышает продукцию сосудистого фактора
роста (VEGF), что приводит к активации вазопролиферативных процессов.
Помимо этого, ФНОα – провоспалительный
цитокин, определяющий развитие синовиального воспаления и остеокласт-опосредованной
костной деструкции при артритах [1, 6–12].
При ПсА, как и при многих других заболеваниях, сопровождающихся иммунными нарушениями, наблюдается патологическое образование ИЛ12 и
ИЛ23. О роли ИЛ12 в патогенезе артрита свидетельствует ряд клинических исследований. Было выявлено, что
уровень ИЛ12 коррелирует с уровнями ФНОα, ИЛ8 и ИЛ10. Повышенное содержание ИЛ1, ИЛ2, ИЛ10, ИФНγ и
ФНОα обнаружено в синовиальной ткани у пациентов с ПсА. Описаны случаи тяжелого обострения артрита в
ответ на введение экзогенного ИЛ12 у пациентов с РА. Недавно опубликованы исследования, указывающие на наличие связи между генетическими вариантами
рецептора к ИЛ23 и развитием ПсА. ИЛ12 и ИЛ23
представляют собой гетеродимерные цитокины, состоящие из двух субъединиц гликозилированных протеинов, связанных дисульфидными мостиками и имеющих общую субъединицу р40. При связывании общей субъединицы p40 с субъединицей p35 образуется ИЛ12, при связывании с субъединицей p19 – ИЛ23, каждая из этих субъединиц названа в соответствии
со своей молекулярной массой. Эти цитокины продуцируются преимущественно макрофагами и дендритными клетками и оказывают действие путем связывания с двухцепочечными гетеродимерными рецепторными комплексами, экспрессируемыми на поверхности CD4+ T-лимфоцитов и естественных киллеров (NK-клетки). Через общую субъединицу
p40 ИЛ12 и ИЛ23 связываются с цепью 1 рецептора к
ИЛ12, вызывая первичное взаимодействие цитокина с рецептором.
Специфичность сигнала обеспечивается связыванием
уникальной субъединицы каждого цитокина с уникальной субъединицей рецепторного комплекса: ИЛ12p35 связывается с рецептором 2 к ИЛ12, а ИЛ23p19 – с рецептором к ИЛ23, запуская внутриклеточную сигнализацию и активируя клетки, несущие рецепторы. ИЛ23 стимулирует клетки Th17, которые начинают продуцировать провоспалительные факторы, включая ИЛ17, которые также стимулируют образование других провоспалительных агентов. Так как ИЛ12 и ИЛ17 играют важную роль в патогенезе псориаза, целевое воздействие на эти цитокины может способствовать нормализации
структуры кожи. Это подтверждается данными экспериментов на животных.
Значимость ИЛ12 и ИЛ23 была доказана при проведении
генетического анализа, продемонстрировавшего, что предрасположенность к развитию псориаза связана с изменениями гена IL12B (кодирующего рецепторы ИЛ23) [1, 6–9]. Таким образом, патогенетической основой развития псориаза является активация клеточного иммунитета в коже и синовии у лиц с врожденной предрасположенностью под воздействием
провоцирующих факторов. Возникающая при этом
гиперпродукция провоспалительных цитокинов, хемокинов вызывает дисбаланс ключевых про- и противовоспалительных цитокинов, таких как ФНОα, ИЛ12, ИЛ23, ИЛ17, ИЛ1, ИЛ1β, ИЛ6 и хемокины. Этот дисбаланс приводит к дебюту заболевания или развитию в последующем его рецидивов [1, 6–9].
В большинстве случаев (67–70%) ПсА возникает уже на
фоне существующих кожных проявлений псориаза. У 10%
больных суставной и кожный синдромы возникают одновременно, а у остальной части пациентов (около 20%) поражение суставов опережает появление поражений кожи на несколько недель, месяцев и даже десятков лет. Заболевание может начаться остро, подостро или развиваться постепенно.
Обычно суставной синдром возникает остро, реже – подостро в виде стойкой артралгии с присоединением у каждого 2-го больного ярко выраженных признаков воспаления.
К типичным клиническим особенностям ПсА относят:
асимметричное поражение суставов; вовлечение в процесс дистальных межфаланговых суставов кистей и стоп, сопровождающееся изменением их формы и сочетающееся с припухлостью околосуставных мягких тканей и синюшно-багровой окраской кожи над ними, что создает картину «симптома редиски», артрит I пальцев кистей и стоп; «осевой» характер поражения суставов кистей и стоп (одновременное поражение пястно-фалангового, проксимального и дистального
межфаланговых суставов одного и того же пальца),
припухлость околосуставных мягких тканей и своеобразную синюшно-багровую окраску кожи в области пораженныхсуставов с развитием «симптома сосиски», ахиллобурсит, подпяточный бурсит, вызывающие боль в области пяток(талалгия); боль в области прикрепления связок и сухожилий (энтезопатия); поражение малоподвижных суставов (грудино-ключичных, акромиально-ключичных); остеолиз суставов кистей и стоп с развитием мутилирующего (обезображивающего)
артрита; рентгенологические признаки асимметричного сакроилиита и спондилита [1, 11, 12].
Системные проявления включают поражение органа
зрения в виде конъюнктивита, иридоциклита, реже – эписклерита.
Возможно развитие общих проявлений (потеря
массы тела, амиотрофия). При тяжелой и злокачественной формах течения ПсА могут наблюдаться поражение сердца по типу миокардита и эндокардита с вовлечением клапанного аппарата (чаще аортального клапана с развитием аортита), поражение почек (нефропатия, вторичный амилоидоз), печени (гепатит), генерализованная лимфаденопатия, синдром
Рейно, вовлечение в процесс нервной системы (полиневрит) и др. [1, 2, 12].
Основная цель фармакотерапии ПсА – достижение ремиссии или минимальной активности заболевания (артрита, спондилита, энтезита, дактилита, кожных проявлений псориаза), замедление или предупреждение рентгенологического прогрессирования, увеличение продолжительности и качества жизни пациентов, а также снижение риска возникновения коморбидных заболеваний [12–16].
Для лечения ПсА применяют НПВП, глюкокортикоиды
(ГК), главным образом внутрисуставные, базисные противовоспалительные препараты (БПВП), таргетные синтетические БПВП (или блокаторы сигнальных путей) и генноинженерные биологические препараты (ГИБП). НПВП – препараты первой линии терапии при активном ПсА, их назначают в сочетании с внутрисуставным введением ГК или без него. Эффективность лечения оценивают каждые 3–6 мес [12–16].
В последние десятилетия для лечения ПсА с успехом используются БПВП. Препаратом первой линии является метотрексат (МТ), оказывающий благоприятное влияние на суставной и кожный компоненты заболевания. МТ назначают внутрь в дозе от 7,5 до 15 мг/нед. При увеличении дозы МТ до 20–25 мг/нед используют его внутримышечное или подкожное введение в комбинации с фолиевой кислотой (20 мкг/сут в те дни, когда МТ не применяют). Доказана эффективность лефлуномида для замедления суставных деструкций и уменьшения выраженности кожных проявлений псориаза.
Доза лефлуномида – 100 мг/сут в течение первых 3 дней, затем– по 20 мг/сут. Применяют также салазопроизводные(сульфасалазин). Начинают лечение с 500 мг/сут в течение недели, затем дозу повышают на 500 мг/сут каждую неделю до терапевтической (2–3 г/сут); поддерживающая доза – 0,5–1,0 г/сут. Хорошо зарекомендовал себя в лечении кожных проявлений
псориаза циклоспорин А. Его суточная доза составляет
2,5–3,0 мг/кг, в процессе лечения необходим контроль уровня креатинина сыворотки крови. При неэффективности БПВП могут быть использованы таргетные синтетические БПВП – апремиласт, ингибитор фосфодиэстеразы 4 (ФДЭ4), зарегистрированный для лечения псориаза и ПсА [12–17].
Несмотря на сложность и многогранность, патогенез
воспаления при ПсА имеет ключевые звенья. Одним из этих звеньев является ФДЭ4 – энзим, участвующий в метаболизме циклического аденозинмонофосфата (цАМФ) в иммунных клетках, регулирующих воспаление, а также катализирующий переход цАМФ в его неактивную форму – АМФ. Ингибиторы ФДЭ4 тормозят разрушение цАМФ и способствуют поддержанию его высокого внутриклеточного уровня, что снижает активность провоспалительных функций клеток.
Хотя семейство ФДЭ состоит из 11 изоформ, ФДЭ4 является цАМФ-специфической и преобладающей изоформой, которая экспрессируется иммунными клетками воспаления.
ФДЭ4 – основной регулятор метаболизма цАМФ практически во всех провоспалительных и структурных клетках, вовлеченных в хроническое воспаление при ПсА [11, 17].
Апремиласт ингибирует внутри клетки ФДЭ4, что ведет
к подавлению воспалительной реакции за счет снижения
продукции ФНОα, ИЛ12, ИЛ23, ИЛ17, ИЛ22 и других провоспалительных цитокинов, а также изменения уровней некоторых противовоспалительных цитокинов, например ИЛ6, ИЛ10. В клинических исследованиях у больных ПсА апремиласт значительно модулировал, но полностью не ингибировал белки плазмы крови: ИЛ1α, ИЛ6, ИЛ8, моноцитарный хемоаттрактантный белок 1, макрофагальный белок воспаления 1β, матриксную металлопротеиназу 3 и ФНОα [14, 15]. Через 40 нед лечения апремиластом отмечено снижение концентрации ИЛ17 и ИЛ23 и повышение содержания ИЛ10 в плазме крови. У больных псориазом апремиласт уменьшал очаговые эпидермальные утолщения пораженных
участков кожи, инфильтрацию клетками воспаления и
экспрессию провоспалительных генов, включая гены индуцируемой синтазы оксида азота (iNOS), ИЛ12/ИЛ23p40, ИЛ17A, ИЛ22 и ИЛ8 (рис. 2) [17–18].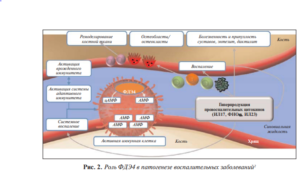
Апремиласт – пероральный ингибитор ФДЭ4, представитель нового класса малых молекул (блокаторы сигнальных путей) в лечении псориаза и ПсА. Препарат применяется для терапии бляшечного псориаза средней и тяжелой степени у взрослых при недостаточной эффективности, противопоказаниях к использованию БПВП или их непереносимости, включая циклоспорин, МТ или лекарственные средства, используемые вместе с ультрафиолетовым облучением А, а также при лечении активного ПсА у взрослых в монотерапии или в комбинации с БПВП при недостаточном ответе на предшествующую терапию БПВП или ее непереносимости [13–16]. Также апремиласт может быть назначен в тех случаях, когда терапия ГИБП не показана (инфекции, особенности введения ГИБП) либо неэффективна. Апремиласт может применяться у больных с коморбидными заболеваниями
(например, метаболическим синдромом, повышенным
риском гепатотоксичности и др.) [13–16].
Особыми клиническими проявлениями ПсА являются
дактилит и энтезит, которые существенно ухудшают качество жизни пациентов и плохо поддаются лечению [1, 12].
Резистентность дактилита и энтезита к терапии объясняется несколькими факторами. Так, некоторые исследователи считают, что она связана с наличием в области воспаления аваскулярных зон (сухожилия, капсулы и др.), в которые затруднена доставка активных действующих веществ лекарственных средств. Более того, дактилит и энтезит ассоциируются с вовлечением в воспаление многих цитокинов, концентрация ряда которых не уменьшается при подавлении воспаления с применением блокаторов других цитокинов. Показано, что уровень ИЛ17A, ИЛ12/23 остается стабильным даже после подавления активности ФНОα [19]. В связи с этим представляется перспективным применение ингибиторов ФДЭ4 (апремиласт), которые одновременно прерывают транскрипцию многих провоспалительных цитокинов и блокируют внутриклеточный механизм ее реализации. Это приводит к подавлению концентрации цитокинов, в том числе в аваскулярных зонах. Такой подход перспективен в лечении дактилита и энтезита, являющихся частыми и тяжелыми проявлениями
ПсА [1, 12, 18, 20, 21].
В рандомизированных клинических исследованиях
(PALACE 1–3) было доказано, что при ПсА апремиласт
эффективен в отношении периферического артрита,
псориаза, а также достоверно повышает физическую активность пациентов и улучшает качество жизни. Ответ
по ACR20, ACR50 и ACR70 наблюдался у 61,3; 30,7 и 12%
пациентов через 1 год терапии и у 66,5; 37,3 и 21% через 2 года [22].
Апремиласт уменьшает выраженность симптомов дактилита и энтезита при ПсА. Эффект доказанно сохраняется в течение 3 лет терапии препаратом. Апремиласт включен в рекомендации EULAR и GRAPPA для лечения активного периферического артрита,
дактилита, энтезита, псориаза (в том числе псориаза ногтей) у пациентов с неэффективностью непереносимостью БПВП или хотя бы одного ГИБП [15, 16, 22–24]. Высокая частота коморбидных состояний при ПсА, в частности хронической обструктивной болезни легких (ХОБЛ) у курильщиков, делает предпочтительным применение у таких больных ингибиторов ФДЭ4, которые положительно влияют как на суставной синдром, так и на поражение легких, т. е. оказывают плейотропный эффект.
Безопасность и эффективность апремиласта изучалась
в ходе многоцентровых рандомизированных двойных слепых плацебоконтролируемых регистрационных исследований III фазы ESTEEM, в которых участвовали 1257 пациентов с хроническим вульгарным псориазом умеренной – тяжелой степени. Пациенты были рандомизированы на группы в соотношении 2:1 для получения апремиласта 30 мг дважды в день и плацебо. К 16-й неделе 75% улучшения по шкале Psoriasis Area and Severity Index (PASI-75 – основной критерий эффективности терапии) достигли 33,1% пациентов
в исследовании ESTEEM I и 28% в исследовании
ESTEEM II, что достоверно выше, чем в группе сравнения
(5,3 и 5,8% соответственно; р<0,0001). Нежелательные реакции (НР), носившие легкий или умеренный характер, ограничивались тошнотой и рвотой и проходили в течение 1 мес после начала приема препарата [25–28].
Полученные данные были подтверждены в ходе другого
исследования III фазы – NCT01172938, в котором изучалась эффективность апремиласта у 504 пациентов с псориазом и ПсА при длительном применении. Через 52 нед доля пациентов, которые ответили на лечение апремиластом 20 или 30 мг дважды в день, увеличилась до 63 и 54,6% соответственно.
Показано, что на фоне приема препарата положительная
динамика кожного процесса (регресс высыпаний,
уменьшение интенсивности окраски бляшек, шелушения и интенсивности зуда) сохранялась в течение 52 нед. Кроме того, у пациентов было отмечено уменьшение/полное исчезновение отечности и болезненности суставов, в том числе при дактилите и энтезите [25, 26].
С осторожностью апремиласт следует применять у пациентов с редкими наследственными нарушениями в виде непереносимости галактозы, с врожденной недостаточностью лактазы или нарушениями всасывания глюкозы-галактозы (препарат содержит лактозу); с почечной недостаточностью тяжелой степени тяжести; с низкой массой тела.
2
Оригинальный рисунок автора (Трофимов Е.А.).
Апремиласт назначают внутрь независимо от времени приема пищи. Рекомендуемая доза – по 30 мг 2 раза в
сутки с интервалом в 12 ч. Требуется начальное титрование дозы, как показано в таблице. В случае перерыва в лечении повторного титрования не
требуется

У пациентов с почечной недостаточностью легкой или
средней степени тяжести нет необходимости в изменении
дозы. Дозу апремиласта следует уменьшить до 30 мг 1 раз в сутки у больных с тяжелой почечной недостаточностью
(клиренс креатинина <30 мл/мин при оценке по формуле
Кокрофта–Голта). При начальном титровании рекомендуется принимать только утреннюю дозу и пропускать вечернюю.
Нет необходимости в изменении дозы у пациентов с
печеночной недостаточностью и пожилых больных.
Наиболее частыми НР в ходе клинических исследований
III фазы ESTEEM 1 (NCT01194219) и ESTEEM 2
(NCT01232283) были нарушения со стороны ЖКТ в виде
учащения стула (15,7%) и тошноты (13,9%). Эти нарушения были в основном легкой или средней степени тяжести, и только в 0,3% случаев были расценены как тяжелые. Данные НР возникали преимущественно в первые 2 нед лечения и обычно исчезали через 4 нед. Другими НР были инфекции верхних дыхательных путей (8,4%), головная боль (7,9%) и головная боль напряжения (7,2%). В целом большинство НР были легкой или средней степени тяжести. Реакции гиперчувствительности наблюдались исключительно
редко. НР зарегистрированы в ходе 5 клинических исследований апремиласта при ПсА (1945 пациентов) и псориазе (1184 пациента) [27–30].
Совместное применение с мощным индуктором изофермента цитохрома P450 3A4 (CYP3A4) рифампицином ведет к ослаблению системного воздействия и уменьшению эффективности апремиласта. Поэтому не рекомендуется комбинированное использование мощных индукторов изофермента
CYP3A4 (например, рифампицин, фенобарбитал,
карбамазепин, фенитоин и препараты зверобоя продырявленного) с апремиластом. При одновременном повторном назначении апремиласта и рифампицина AUC и Cmax апремиласта снижаются соответственно на 72 и 43%. В случаях комбинирования апремиласта с мощными индукторами изофермента CYP3A4 (например, рифампицином) клинический ответ может снижаться.
В клинических исследованиях апремиласт использовали
одновременно со средствами местной терапии (ГК, дегтярный шампунь, препараты с содержанием салициловой кислоты для обработки волосистой части головы) и узкополосной средневолновой фототерапией. Апремиласт можно сочетать с сильными ингибиторами изофермента CYP3A4, такими как кетоконазол.
При этом не выявлено клинически значимого лекарственного взаимодействия. Не обнаружено фармакокинетического лекарственного взаимодействия и между апремиластом и МТ у пациентов с ПсА, как и между апремиластом и пероральными контрацептивами, содержащими этинилэстрадиол и норгестимат [10]. Апремиласт можно принимать вместе со всеми указанными лекарственными средствами.
Полученные к настоящему времени данные контролируемых исследований (ESTEEM 1, 2 и PALACE 1–4) свидетельствуют об эффективности и безопасности апремиласта при лечении псориаза и ПсА. В отличие от БПВП апремиласт имеет уникальную структуру, препятствующую развитию НР, связанных с цитотоксичностью. В противоположность ГИБП он не обладает иммуногенностью, а значит, обеспечивает
долгосрочный стабильный эффект терапии при длительном применении. Благодаря альтернативным путям внутриклеточной передачи сигнала и молекулярным особенностям происходит преимущественное накопление апремиласта в
воспаленных тканях [23, 30]. При ПсА препарат обеспечивает быстрое и стойкое улучшение основных клинических проявлений заболевания, а пероральное его применение в сочетании с низкой частотой местных и системных иммунных реакций способствует приверженности пациентов лечению. Апремиласт уменьшает не только активность артрита, но и
выраженность кожных проявлений псориаза.
Заключение. Апремиласт, ингибитор ФДЭ4, является
представителем нового класса малых молекул, или таргетныхсинтетических БПВП, в лечении псориаза и ПсА. В международных рандомизированных клинических исследованиях (РКИ) было показано, что апремиласт эффективен при различных проявлениях ПсА (периферический артрит, энтезит, дактилит, спондилит), а также среднетяжелом, тяжелом бляшечном псориазе, в том числе псориазе проблемных локализаций.
Для апремиласта характерно благоприятное соотношение
«риск/польза» при длительном применении: стабильный
эффект терапии, отсутствие иммуногенности, признаков
гепато-, нефро- и кардиотоксичности, низкий риск развития серьезных инфекций. Апремиласт продемонстрировал сходную краткосрочную и долгосрочную (в течение 5 лет) эффективность и безопасность в российский когорте пациентов
с ПсА, включенных в международные РКИ. В соответствии с Федеральными клиническими рекомендациями по лечению ПсА апремиласт рекомендуется назначать больным с высокой активностью периферического артрита, энтезита и
дактилита при неэффективности/непереносимости предшествующей терапии БПВП или противопоказаниями к лечению БПВП, а также с неэффективностью/непереносимостью ГИБП или противопоказаниями к терапии ГИБП.
ЛИТЕРАТУРА
1. Мазуров ВИ. Болезни суставов. Руководство
для врачей. Санкт-Петербург:
СпецЛит; 2008. 408 c. [Mazurov VI. Bolezni
sustavov. Rukovodstvo dlya vrachei [Diseases
of the joints. A guide for physicians]. SaintPetersburg:
SpetsLit; 2008. 408 p.]
2. Parisi R, Symmons D P, Griffiths C E,
Ashcroft DM. Global epidemiology of psoriasis:
A systematic review of incidence and
prevalence. J Invest Dermatol. 2013 Feb;133(2):
377-85. doi: 10.1038/jid.2012.339.
Epub 2012 Sep 27.
3. Eder L, Cohen AD, Feldhamer I, et al.
The epidemiology of psoriatic arthritis in
Israel – a population-based study. Arthritis Res
Ther. 2018 Jan 2;20(1):3. doi: 10.1186/s13075-
017-1497-4.
4. Sewerin P, Hoyer A, Schneider M, et al.
ОБЗОРЫ
Inconsistency between Danish incidence and
prevalence data about psoriatic arthritis (PsA).
Ann Rheum Dis. 2018 Jan 2. pii:
annrheumdis-2017-212817. doi: 10.1136/
annrheumdis-2017-212817. [Epub ahead of
print]
5. Псориатический артрит. https://psoriazov.net/vidy-psoriaza/klassifikaciya-psoriaza.html
[Psoriatic arthritis. https://psoriazov.net/vidy-psoriaza/klassifikaciya-psoriaza.html]
6. Hawkes JE, Chan TC, Krueger JG.
Psoriasis pathogenesis and the development
of novel targeted immune therapies. J Allergy
Clin Immunol. 2017 Sep;140(3):645-653. doi:
10.1016/j.jaci.2017.07.004.
7. Paine A, Ritchlin C. Altered Bone
Remodeling in Psoriatic Disease: New
Insights and Future Directions. Calcif Tissue
Int. 2018 Jan 12. doi: 10.1007/s00223-017-
0380-2. [Epub ahead of print].
8. Eyre S, Orozco G, Worthington J. The
genetics revolution in rheumatology: large
scale genomic arrays and genetic mapping.
Nat Rev Rheumatol. 2017 Jul;13(7):421-432.
doi: 10.1038/nrrheum.2017.80.
Epub 2017 Jun 1.
9. Yago T, Nanke Y, Kawamoto M, et al.
IL-23 and Th17 Disease in Inflammatory
Arthritis. J Clin Med. 2017 Aug 29;6(9).
pii: E81. doi: 10.3390/jcm6090081.
10. Мазуров ВИ, Трофимов ЕА. Ревматология.
Фармакотерапия без ошибок: руководство
для врачей. Москва: Е-ното;
2017. 528 с. [Mazurov VI, Trofimov EA.
Revmatologiya. Farmakoterapiya bez oshibok:
rukovodstvo dlya vrachei [Rheumatology.
Pharmacotherapy without errors: a guide for
physicians]. Moscow: E-noto; 2017. 528 p.].
11. Alwan W, Nestle FO. Pathogenesis and
treatment of psoriasis: Exploiting pathophysiological
pathways for precision medicine. Clin
Exp Rheumatol. 2015 Sep-Oct;33(5 Suppl 93):
S2-6. Epub 2015 Oct 15
12. Молочков ВА, Бадокин ВВ, Альбанова
ВИ. Псориаз и псориатический артрит.
Москва: Товарищество научных изданий
КМК; 2007. 300 с. [Molochkov VA,
Badokin VV, Al’banova VI. Psoriaz i psoriaticheskii
artrit [Psoriasis and psoriatic arthritis].
Moscow: Tovarishchestvo nauchnykh izdanii
KMK; 2007. 300 p.]
13. Федеральные клинические рекомендации
по ведению больных псориазом.
http://mzdrav.rk.gov.ru/file/Psoriaz_0505201
4_Klinicheskie_rekomendacii.pdf. [Federal
clinical guidelines for the management of
psoriasis patients. http://mzdrav.rk.gov.ru/file/
Psoriaz_05052014_Klinicheskie_rekomendacii.pdf]
14. Федеральные клинические рекомендации
по ведению больных псориатическим
артритом. http://www.ismos.ru/guidelines/doc/
psoriaticheskij_artrit.pdf. [Federal clinical
guidelines for the management of patients
with psoriatic arthritis. http://www.ismos.ru/
guidelines/doc/psoriaticheskij_artrit.pdf]
15. Coates LC, Kavanaugh A, Mease PJ,
et al. Group for Research and Assessment of
Psoriasis and Psoriatic Arthritis (GRAPPA):
Treatment Recommendations for Psoriatic
Arthritis 2015. Arthritis Rheumatol. 2016 May;
68(5):1060-71. doi: 10.1002/art.39573.
Epub 2016 Mar 23
16. Gosses L, Smolen JS, Ramiro S, et al.
European Leaque Against Rheumatism
(EULAR) recommendations for the management
of psoriatic arthritis with pharmacological
therapies: 2015 update. Ann Rheum Dis.
2016 Mar;75(3):499-510. doi: 10.1136/
annrheumdis-2015-208337. Epub 2015 Dec 7.
17. Sakkas LI, Mavropoulos A, Bogdanos DP.
Phosphodiesterase 4 Inhibitors in Immunemediated
Diseases: Mode of Action, Clinical
Applications, Current and Future Perspectives.
Curr Med Chem. 2017;24(28):3054-3067.
doi: 10.2174/0929867324666170530093902.
18. Gladman DD, Kavanaugh A,
Gomez-Reino JJ, et al. Apremilast treatment
and long-term (up to 156 weeks) improvements
in dactylitis and enthesitis in patients
with psoriatic arthritis: analysis of a large
database of the phase III clinical development
program. Ann Rheum Dis. 2017;76(suppl2):942.
19. Гайдукова ИЗ, Ребров АП, Апаркина АВ,
Хондкарян ЭВ. Концентрация интерлейкина-17α
остается стабильно высокой у
больных анкилозирующим спондилитом,
получающих ингибиторы фактора некроза
опухоли α в течение года. Терапевтический
архив. 2017;89(4):80-5. [Gaidukova IZ,
Rebrov AP, Aparkina AV, Khondkaryan EV.
The concentration of interleukin-17α
remains high in patients with ankylosing
spondylitis receiving inhibitors of tumor
necrosis factor α in the course of the year.
Terapevticheskii arkhiv. 2017;89(4):80-5.
(In Russ.)].
20. Armstrong A, Levi E. Real-world clinical
experience with apremilast in a large us retrospective
cohort study of patients with moderate
to severe plaque psoriasis. J Drugs
Dermatol. 2017 Dec 1;16(12):1240-1245.
21. Dattola A, Del Duca E, Saraceno R, et al.
Safety evaluation of apremilast for the treatment
of psoriasis. Expert Opin Drug Saf. 2017;
Mar;16(3):381-385. doi: 10.1080/14740338.
2017.1288714. Epub 2017 Feb 7.
22. Kavanaugh A, Gladman DD,
Gomez-Reino JJ, et al. Durability of apremilast
response in patients with psoriatic arthritis:
long-term (208-week) results from the
PALACE 1 trial. Ann Rheum Dis. 2017;
76(suppl2):936.
23. Reich K, Gooderham M, Bewley A, et al.
Safety and efficacy of apremilast through 104
weeks in patients with moderate to severe
psoriasis who continued on apremilast or
switched from etanercept treatment: findings
from the LIBERATE study. J Eur Acad
Dermatol Venereol. 2017 Dec 8. doi: 10.1111/
jdv.14738. [Epub ahead of print]
24. Armstrong AW, Robertson AD, Wu J,
et al. Undertreatment, treatment trends, and
treatment dissatisfaction among patients with
psoriasis and psoriatic arthritis in the United
States: Findings from the National Psoriasis
Foundation surveys, 2003–2011. JAMA
Dermatol. 2013 Oct; 149(10):1180-5. doi:
10.1001/jamadermatol.2013.5264.
25. Kavanaugh A, Mease PJ,
Gomez-Reino JJ, et al. Longterm (52-week)
Results of a Phase III Randomized,
Controlled Trial of Apremilast in Patients
with Psoriatic Arthritis. J Rheumatol. 2015
Mar;42(3):479-88. doi: 10.3899/jrheum.
140647. Epub 2015 Jan 15.
26. Kavanaugh A, Mease PJ, Gomez-Reino JJ,
et al. Treatment of psoriatic arthritis in a
phase 3 randomised, placebo-controlled trial
with apremilast, an oral phosphodiesterase 4
inhibitor. Ann Rheum Dis. 2014 Jun;73(6):1020-6.
doi: 10.1136/annrheumdis-2013-205056.
Epub 2014 Mar 4.
27. Papp K, Reich K, Leonardi CL, et al.
Apremilast, an oral phosphodiesterase 4
(PDE4) inhibitor, in patients with moderate
to severe plaque psoriasis: Results of a phase
III, randomized, controlled trial (efficacy and
safety trial evaluating the effects of apremilast
in psoriasis [ESTEEM] 1). J Am Acad
Dermatol. 2015 Jul;73(1):37-49. doi: 10.1016/
j.jaad.2015.03.049.
28. Paul C, Cather J, Gooderham M, et al.
Efficacy and safety of apremilast, an oral
phosphodiesterase 4 inhibitor, in patients with
moderate to severe plaque psoriasis over 52
weeks: A phase III, radomized, controlled
trial (ESTEEM 2). Br J Dermatol. 2015 Dec;
173(6):1387-99. doi: 10.1111/bjd.14164.
Epub 2015 Nov 7.
29. Crowley J, Thaci D, Joly P, et al. Longterm
safety and tolerability of apremilast in
patients with psoriasis: Pooled safety analysis
for ≥156 weeks from 2 phase 3, randomized,
controlled trials (ESTEEM 1 and 2). J Am
Acad Dermatol. 2017 Aug;77(2):310-317.e1.
doi: 10.1016/j.jaad.2017.01.052.
Epub 2017 Apr 14.
30. Bissonnette R, Pariser DM, Wasel NR,
et al. Apremilast, an oral phosphodiesterase-4
inhibitor, in the treatment of palmoplantar
psoriasis: Results of a pooled analysis from
phase II PSOR-005 and phase III Efficacy
and Safety Trial Evaluating the Effects of
Apremilast in Psoriasis (ESTEEM) clinical
trials in patients with moderate to severe psoriasis.
J Am Acad Dermatol. 2016 Jul;75(1):
99-105. doi: 10.1016/j.jaad.2016.02.1164.
Epub 2016 Mar 24.
Поступила 5.01.2018
Исследование поддержано «Селджен Интернэшнл Холдингс Корпорэйшн». Авторы несут полную ответственность за
предоставление окончательной версии рукописи в печать. Все авторы принимали участие в разработке концепции статьи и
написании рукописи. Окончательная версия рукописи была одобрена всеми авторами.